|
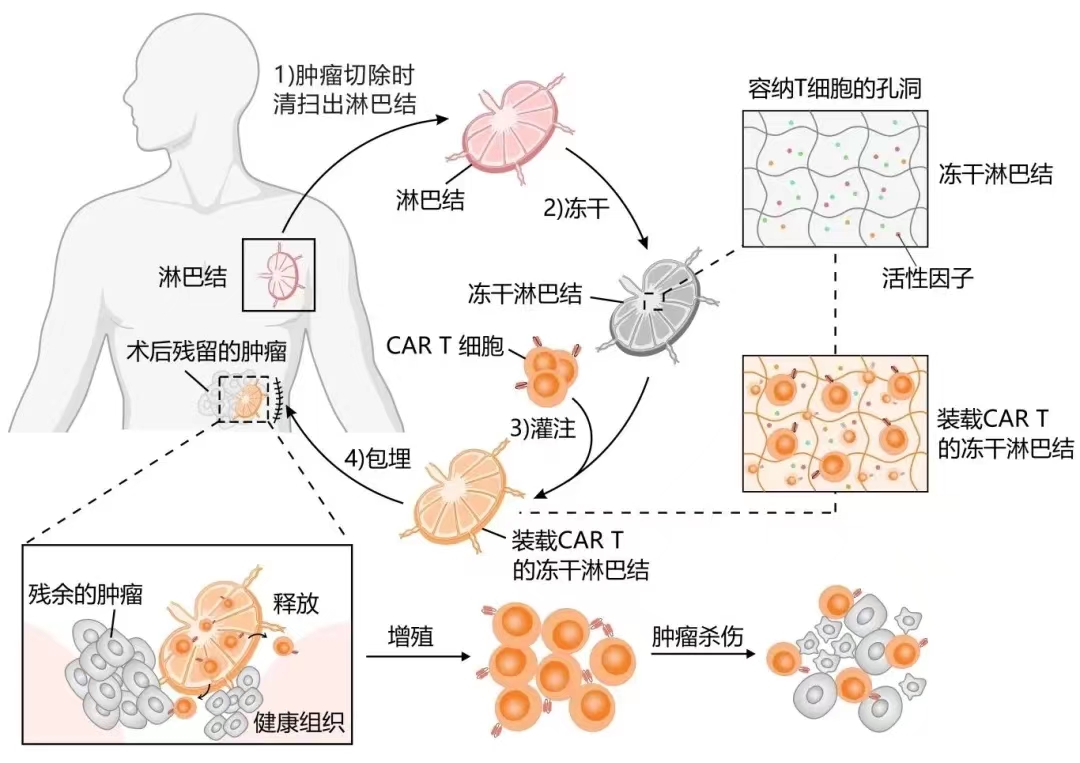
冻干是市面上一种常见的保存新鲜蔬果的方式,通过先低温后真空的处理方法将蔬果内的水分由冰直接升华成水蒸气,从而实现脱水保鲜的效果。那么人们是否也可以冻干一些机体组织,保持其内部的有效成分和结构,作为一种活性材料充分发挥其自身的特性,并用于生物医药领域呢? 日前,浙江大学药学院、浙江大学金华研究院顾臻教授、李洪军研究员团队联合浙江大学医学院附属第一医院赵鹏主任医师、陈栋主任医师团队,在国际上首次提出利用冷冻干燥的淋巴结组织提升抗肿瘤药物的疗效。这项成果于3月6日,发表于国际知名期刊《自然·材料》上。 就地取材,一举两得 近年来,细胞药物用作肿瘤靶向治疗方兴未艾。比如,通过给免疫T细胞加装“探头”,合成能够精准识别并定点清除肿瘤细胞的嵌合抗原受体T细胞(又称CAR T细胞),在临床上已被用于血液瘤的治疗,取得显著疗效。然而CAR T细胞如何在实体肿瘤部位持久且高效地发挥作用,一直是个老大难问题。 “我们就在思考,能否用体内的一些肌体组织来装载CAR T细胞呢?”顾臻介绍,我们想到了肿瘤手术中经常需要进行清扫的淋巴结,这样就地取材,还能避免由于外源载体带来的排异问题。而这些切除的淋巴结本身也是人体内非常重要的免疫器官,好比是免疫系统中的“兵工厂”,天然就是一个适合T细胞生存、训练、扩增的场所。“两者的优势是否可以进一步叠加,既让淋巴结保护CAR T细胞,又能促进细胞的抗肿瘤活性,实现一举两得。”顾臻进一步介绍研究思路。
冻干“锁鲜”,优势多效果好 如何让淋巴结留出更多空间装载CAR T细胞?顾臻团队创造性地提出对淋巴结组织进行冷冻干燥的想法。冻干过程中,淋巴结中水分被冻成冰后迅速升华,产生更多容纳T细胞的空腔。冻干后的淋巴结组织具有很强的吸水性,能迅速吸纳CAR T细胞。 冻干淋巴结的效果如何?科研人员通过对比实验发现,装载在冻干淋巴结内的CAR T细胞在与肿瘤细胞共培养3天后,其中CAR T细胞扩增量是人工制备的凝胶载体的3.5倍。培养7天后,冻干淋巴结的实验组可以使T细胞分化出更多的记忆表型,这都预示了使用冻干淋巴结载体可以让CAR T疗法更强效、也更持久。赵鹏表示:“冻干具有‘锁鲜’功能,冻干的淋巴结还将丰富的细胞因子、趋化因子与配体等成分保留了下来,这对CAR T细胞维持活性和功能有着重要作用。” 为此,浙大科研人员对冻干淋巴结技术充满期待。未来,仅需几个小时,就可以完成淋巴结的冻干与细胞药物的装载,甚至在一场外科手术的时间内,载药的冻干淋巴结就可以填埋回肿瘤术后切除的空腔部位,作为一个CAR T细胞储库,源源不断地持续释放药物,以清除局部残留的微小肿瘤,抑制手术后的复发。 “不止于此,冻干组织技术不仅仅能用于改造淋巴结、装载CAR T细胞,也为未来科学研究提供了一种新思路。”陈栋说,冷冻干燥技术还可以拓展到其他组织与器官,制备性能特殊的生物材料用于生物医药领域。(刘海波) |